Dipol des Wassers: Bedeutung, Ursachen und Auswirkungen
Ein Dipol (Di heißt zwei) ist ein Molekül mit zwei verschieden geladenen Polen. Das Molekül hat auf der einen Seite einen positiven Pol, auf der anderen Seite einen negativen Pol. Wasser ist ein Beispiel für ein dipolares Molekül.
Inhalt
- 1 Wie kann man sich den Dipol im Wasser vorstellen?
- 2 Wie entsteht der Dipol im Wasser?
- 3 Wie sieht ein Wassermolekül aus?
- 4 Warum ist Wasser jetzt ein Dipol?
- 5 Dipol-Dipol Wechselwirkungen
- 6 Warum ist der Dipol im Wasser so wichtig für das Leben?
- 7 Was macht Wasser so einzigartig bei seiner Negativität?
- 8 Zusammenfassung
Wie kann man sich den Dipol im Wasser vorstellen?
Die polaren Kräfte können einen Wasserstrahl ablenken. Das kannst du in einem – wirklich einfachen – Versuch zeigen. Du reibst einen Luftballon an einem Baumwoll-T-Shirt, dadurch lädt sich der Luftballon statisch (negativ) auf. Bringst du jetzt den Luftballon mit seiner statischen Elektrizität in der Nähe eines (dünnen) Wasserstrahls, dann bewegt sich der Wasserstrahl zum Ballon hin.
Wie kommt das?
Der Wasserstrahl besteht aus Wasser, also aus ganz vielen Dipolmolekülen. Der Ballon ist negativ geladen. Entgegengesetzte Ladungen ziehen sich an. Kommt der Ballon in die Nähe des Wasserstrahls, dann richten sich die Moleküle des Wasserstrahls aus: Alle Pluspole der Wassermoleküle richten sich in Richtung des negativ geladenen Ballons aus
So kannst du den Wasserstrahl sichtbar ablenken und siehst: Wasser ist ein Dipolmolekül.
Wasser hat doch keine Ladung?
Richtig, Wasser besteht aus ungeladenen Molekülen. Aber Wasser ist ein polares Molekül. Es besitzt einen positiven und einen negativen Pol.
Wie entsteht der Dipol im Wasser?
Polarität entsteht im Wassermolekül (unter anderem) dadurch, dass Elektronen unterschiedlich stark angezogen werden. Denn Wasser besteht aus zwei Wasserstoffatomen und einem Sauerstoffatom.(H2O)
Warum? Das ist jetzt ein bisschen kompliziert. Jedes Atom hat Elektronen. Am liebsten hat jedes Atom acht Außenelektronen. Wasserstoff ist eine Ausnahme. Ihm genügen (wie allen Elementen in der 1 Periode des Periodensystems) zwei Außenelektronen.
Die Kombination H2O ist perfekt, um allen Beteiligten ihren Wunsch nach mehr Außenelektronen zu erfüllen. Ein Sauerstoffatom hat sechs Außenelektronen. Es hätte aber gerne acht Elektronen. Denn nach der Oktett Regel strebt jedes Atom eine vollbesetzte Außenschale an.

Ein Wasserstoffatom hat ein Außenelektron (Ordnungszahl 1). Weiterhin steht es in Periode I des Periodensystems. Diese Elemente wollen nur zwei Außenelektronen haben. Denn alle Elemente in Periode 1 haben lediglich eine Schale. Und die erste Schale kann bei jedem Element nur 2 Elektronen aufnehmen.
Das heißt jetzt…
Das Wasserstoff hat nur ein Elektron, da Ordnungszahl 1 – versucht dennoch ein zweites zu bekommen. Das bedeutet, wenn Sauerstoff und Wasserstoff aufeinander treffen, sind beide äußerst reaktionsfreudig.

Probieren wir aus, wenn ein Sauerstoffatom auf ein Wasserstoffatom trifft.
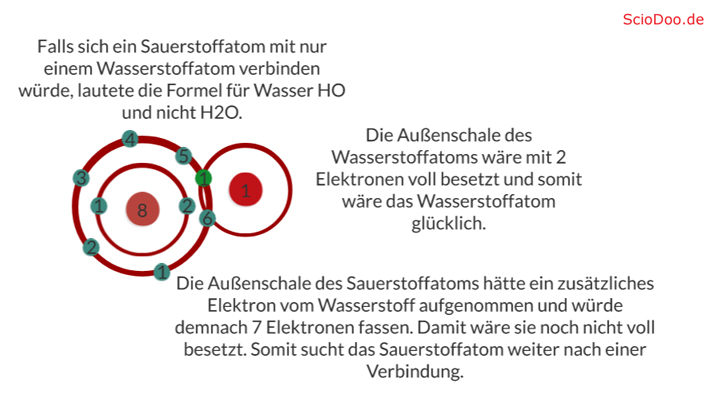
Das Sauerstoffatom wird mit nur einem Wasserstoffatom nicht glücklich sein und sucht weiter nach einem Reaktionspartner.

2 Wasserstoffatome treffen auf ein Sauerstoffatom. Und schließlich gehen alle eine Verbindung ein. Der Sauerstoff und die beiden Wasserstoffe stellen sich ihre Elektronen gegenseitig zur Verfügung, somit sind alle Atome glücklich.
Nun besitzt Sauerstoff in der Wasserverbindung (H2O) zwei Außenelektronen, welche es vom Wasserstoff genommen hat. Und der Wasserstoff hat ebenfalls eine voll besetzte Außenschale.
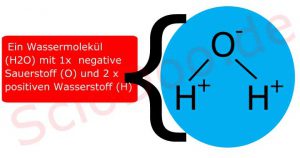
Wie sieht ein Wassermolekül aus?

Bei dem Molekül Wasser, H2O, steht der Sauerstoff in der Mitte, der Wasserstoff steht rechts und links davon.
Sauerstoff und Wasserstoff teilen sich jeweils zwei Elektronen zu beiden Seiten. Hier spricht man von Elektronenpaaren. Jetzt haben alle drei Atome (ein Sauerstoffatom, zwei Wasserstoffatome) so viele Außenelektronen, wie sie möchten: Sauerstoff hat acht Außenelektronen, der Wasserstoff hat jeweils zwei Außenelektronen.
Das Sauerstoffatom stellt von seinen sechs Außenelektronen zwei dem Wasserstoff zur Verfügung. Mit jedem Wasserstoff teilt es sich jeweils ein Elektron. Jedes Wasserstoffatom stellt sein einziges Außenelektron zur Verfügung und teilt es mit dem Sauerstoffatom.
Jeweils ein Wasserstoff steht also rechts und links vom Sauerstoff und auf jeder Seite teilen sie sich ein gemeinsames Elektronenpaar. Durch das gemeinsame Elektronenpaar werden sie zusammengebunden.
Warum ist Wasser jetzt ein Dipol?
Weil das Sauerstoffatom die Elektronen deutlich stärker anzieht als der Wasserstoff. Sauerstoff besitzt eine Elektronegativität von 3,5 und Wasserstoff von 2,2. Diese kannst du im Periodensystem ablesen. Somit sind die Elektronen (und ihre negative Ladung) nicht gleichmäßig über das Molekül verteilt.
Sauerstoff ist elektronegativer als Wasser, d.h. es zieht stärker Elektronen zu sich. Die Elektronen liegen viel näher am Sauerstoff als am Wasserstoff. Das Sauerstoffatom entreißt den Wasserstoffatomen die Bindungselektronen nicht. Sie werden lediglich in Richtung Sauerstoff verschoben.
Die Elektronen sind negativ, daher entsteht am Sauerstoffatom – eben durch die verschobenen Elektronen – eine negative Teilladung, auch Partialladung genannt. Diese Partialladung wird durch ein kleines Delta gekennzeichnet. Der negative Pol – das Sauerstoffatom – erhält ein negatives Delta.
Da die negativen Elektronen vom Wasserstoffatom weiter weg sind, fehlt diesem Atom eine Ladung. Die beiden Wasserstoffatome bilden also den positiven Pol und werden mit einem positiven Delta gekennzeichnet.
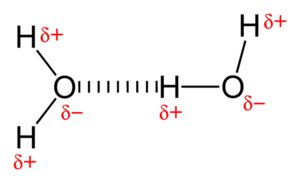
Dipol-Dipol Wechselwirkungen
Dipol-Dipol Wechselwirkungen basieren auf der Grundlage: Gegensätze ziehen sich an. Im Wasser richten sich die einzelnen Moleküle so aus, dass positive und negative Partialladungen eng zusammenkommen. Der partiell negative Sauerstoff des einen Wassermoleküls liegt nahe neben dem partiell positiven Wasserstoffatom des nächsten Moleküls. Diese zwischenmolekulare Kraft wird als Dipol-Dipol-Wechselwirkung beschrieben.
Das heißt jetzt…
Der partiell negative geladene Sauerstoff des einen Moleküls zieht seinen eigenen Wasserstoff an, aber auch den aus benachbarten Molekülen. Man spricht hier von Wasserstoffbrücken – aufgrund der Anziehungskräfte.
Was bringen die Dipol-Dipol Wechselwirkungen?
Sie beeinflussen die Stoffeigenschaften. Die Löslichkeit eines Stoffes in verschiedenen Lösungsmitteln hängt davon ab. Der Schmelz- und Siedepunkt hängt davon ab – je nachdem, wie stark die Anziehungskräfte sind.
Warum ist der Dipol im Wasser so wichtig für das Leben?
Aufgrund dessen, dass der Sauerstoff im Molekül den Wasserstoff aus benachbarten Molekülen anzieht – entstehen die Wasserstoffbrücken zwischen den Molekülen. Dies bewirken Einiges, welches Leben überhaupt erst möglich macht.
1. Anziehungskräfte im Dipol sorgen für die Wasseraufnahme der Pflanzen
Wasser perlt. Es ist eine Flüssigkeit, welche sich in Tropfen bildet. Die Anziehungskräfte sind daran schuld.
Aufgrund der Tropfenform haftet Wasser besser an Oberflächen als jede andere Flüssigkeit und kann so von Pflanzen gut aufgenommen werden.
2. Der Dipol ist die Ursache dafür, dass Leben entstehen konnte
Wenn Stoffen Energie entzogen wird (durch Kälte) ziehen sich die Moleküle zusammen. Dadurch entsteht eine größere Dichte.
Die Anziehungskräfte des Wassermoleküls sorgen allerdings dafür, dass Wasser sich ab 4 Grad Celsius wieder ausdehnt. Eis hat, obwohl es kälter ist, eine kleinere Dichte als Wasser. Dies nennt man Dichteanomalie des Wassers.
Diese ist wichtig und einzigartig. Denn dieser Umstand sorgt dafür, dass Wasser welches 4 Grad Celsius hat, unter das Eis sinkt, weil die Dichte größer ist und das Wasser somit schwerer ist. Dadurch können Seen nicht zufrieren und machen das Leben im Wasser möglich.
Da Leben im Wasser entstand, macht diese Eigenschaft den Ursprung des Lebens überhaupt erst möglich.
3. Der Dipol des Wassers sorgt für den Stoffwechsel der Lebewesen
Wasser ist der Superlöser, da die Anziehungskräfte des Dipols (partielle Sauerstoffladung) Kohäsionskräfte gegenüber anderen Stoffen entwickeln. Damit verändert Wasser die Adhäsionskräfte (Anziehungskräfte innerhalb) der Stoffe, welche im Wasser sind. Die Dichteeigenschaften sämtlicher Stoffe, welche sich in Wasser auflösen, wird demnach verändert.
Durch diese Eigenschaft spielt Wasser die entscheidende Rolle im Stoffwechsel, bei der Verdauung und bei der Zellversorgung. Der Mensch besteht zu 70 % aus Wasser, was mit dessen Lösungseigenschaften zu tun hat.
4. Wasser ist der Superleiter für die Schaltzentrale im Körper
Wasser ist der Superleiter aufgrund des Dipols. Dies spielt wiederum eine wichtige Rolle bei der Übertragung von elektrische Impulse, welche bei der Wahrnehmung (Sehen, Hören, Fühlen, Schmecken usw) entstehen.
Diese Impulse werden durch das Zellinnere, welches zu großem Teil aus Wasser besteht, geleitet und übertragen. Von Zelle zu Zelle findet die elektrische Übertragung statt und landet letztlich im Gehirn, welches wiederum Maßnahmen einleitet. Und diese Übertragung vom Gehirn zur Zielzelle zurück sind ebenfalls elektrische Impulse.
Was macht Wasser so einzigartig bei seiner Negativität?
Oder warum ist CO2 kein polares Molekül?
Weil sich hier die unterschiedlichen Ladungen gegenseitig aufheben. Eigentlich sollte auch C02 ein polares Molekül sein. Es besteht aus einem Kohlenstoffatom (Ordnungszahl 6 Periode 2, Schalenbesetzung: 2 und 4) und zwei Sauerstoffatomen. Demnach braucht der Kohlenstoff 4 Elektronen, um die 8-Schale voll zu bekommen. Sobald Kohlenstoff eine Verbindung mit 2 Sauerstoffatomen eingeht, nimmt es jeweils 2 Außenelektronen vom Sauerstoff und gibt 2×2 zurück.

Der Sauerstoff ist elektronegativer als der Kohlenstoff. Er zieht folglich gemeinsame Elektronen stärker zu sich. Das CO2 Molekül ist jedoch gestreckt, nicht gewinkelt (wie das Wassermolekül). C02 ist ein lineares Molekül. Die einzelnen Dipole sind dadurch symmetrisch angeordnet und heben sich auf. Der gesamte Dipol ist gleich null.
Damit ein Molekül polar ist, muss es:
- Aus Atomen mit unterschiedlichen Elektronegativitäten aufgebaut sein
- Eine asymmetrische Struktur haben.
Zusammenfassung
- Der Dipol des Wassers beschreibt, den Aufbau des Wassers – welches aus zwei unterschiedlichen geladenen Enden besteht.
- Wasser ist eine molekulare Bindung, bestehend aus 2 Teilchen Wasserstoff und einem Sauerstoff, die miteinander verbunden sind.
- Der Dipol des Wassers entsteht, da Sauerstoff eine höhere Elektronegativität besitzt und den Wasserstoff stärker zu sich zieht.
- Und da Sauerstoff auch den Wasserstoff aus den nächsten Wassermolekül anzieht, entstehen Brücken zwischen dem Wasserteilchen.
- Diese Wasserstoffbrücken sind Kräfte – welche zwischen benachbarten Wassermolekülen wirken.
- Diese Kräfte oder Dipol-Dipol Wechselwirkungen beeinflussen die Stoffeigenschaften von sämtlichen Stoffen, welche sich im Wasser befinden.
- Aufgrund dieser Dipol-Kräfte perlt Wasser an der Fensterscheibe oder im Regentropfen an einer Pflanze.
- Aufgrund dieser Eigenschaften ist Wasser nass bzw. fühlt sich nasser an als Öle oder Fette.
- Der Dipol bewirkt die Dichteanomalie des Wassers, wonach Wasser bei unter 4 Grad Celsius seine Dichte ausbreitet, anstatt zu verkleinern.
- Und Wasser wird aufgrund der unterschiedlich geladenen Pole zum Superleiter von Strom. Dies ist wichtig, da das Nervensystem auf die Weitergabe von elektrischen Impulsen von Nervenzelle zu Nervenzelle setzt.
Über den Autor